IMVANEX
Laboratoire : Bavarian Nordic A/S
Le 20 septembre 2024 : ce vaccin est maintenant autorisé dès l'âge de 12 ans.
Le 14 août 2024 : l'émergence du mpox sur le continent africain constitue une urgence de santé publique de portée internationale.
Le laboratoire pharmaceutique Bavarian Nordic a sollicité l’Agence européenne du médicament (EMA) pour étendre l’utilisation de son vaccin antivariolique, Imvanex, aux adolescents de 12 à 17 ans. Cette demande s’appuie sur des données en faveur de l’efficacité et de la sécurité du vaccin pour cette tranche d’âge.
Vaccin commercialisé aux Etats-Unis sous le nom de JYNNEOS et au Canada sous le nom de IMVAMUNE.
Une ou deux doses de ce vaccin se sont avérées très efficaces pour prévenir le mpox et éviter l'hospitalisation. Des données sur l'efficacité vaccinale en vie réelle contre le mpox sont décrites dans le chapitre "Pharmacodynamie".
Description
Vaccin contre la variole de troisième génération, virus modifié de la vaccine d'Ankara, non réplicatif. Autre nom : MVA-BN (Modified Vaccine Ankara ; BN = Bavarian Nordic).
Interchangeabilité
Forme et Présentation
▼ Ce symbole indique que ce vaccin fait l'objet d'une surveillance supplémentaire. Cela permettra d'identifier rapidement de nouvelles informations de sécurité. Il est demandé aux professionnels de santé de signaler tout effet indésirable suspecté.
IMVANEX suspension injectable.
Vaccin antivariolique et anti-variole du singe (virus vivant modifié de la vaccine Ankara).
Suspension de couleur jaune pâle à blanche, transparente à laiteuse.
Nature et contenu de l'emballage extérieur
- 0,5 mL de suspension dans un flacon (en verre de type I) avec un bouchon (caoutchouc bromobutyle).
- Boîtes de 1 flacon unidose, 10 flacons unidoses ou 20 flacons unidoses.
Toutes les présentations peuvent ne pas être commercialisées.
Composition
1. Antigène
Une dose (0,5 mL) contient :
- Virus vivant modifié de la vaccine Ankara – Bavarian Nordic 1, minimum 5 x 107 U. Inf .*
1 Produit sur des cellules d’embryons de poulet.
2. Excipients
- Trométamol
- Chlorure de sodium
- Eau pour préparations injectables
Ce vaccin contient des traces résiduelles de protéines de poulet, benzonase, gentamicine et ciprofloxacine (voir rubrique "Contre-indications").
Indications
Immunisation active contre la variole, le mpox et la maladie causée par le virus de la vaccine chez les personnes âgées de 12 ans et plus (voir rubriques "Mises en garde et précautions d'emploi" et "Pharmacodynamie").
Le 20 septembre 2024, la Commission européenne a autorisé l'utilisation de ce vaccin dès l'âge de 12 ans (au lieu de 18 ans auparavant).
Le 25 juillet 2022, la Commission européenne ajoute deux indications en plus de la prévention de la variole : la prévention du mpox et celle de la maladie causée par le virus de la vaccine.
L’utilisation de ce vaccin doit se faire conformément aux recommandations officielles.
La Haute Autorité de santé recommande la vaccination :
- en priorité, des adultes qui ont eu un contact à risque avec un malade atteint de mpox (maladie encore appelée monkeypox ou "variole du singe") ;
- des hommes ayant des relations sexuelles avec des hommes (HSH) rapportant des partenaires multiples ;
- des personnes trans rapportant des partenaires sexuels multiples ;
- des personnes en situation de prostitution ;
- des professionnels des lieux de consommation sexuelle, quel que soit le statut de ces lieux.
Qu'est-ce qu'une personne-contact à risque de mpox ?
Il y a deux situations à risque :
- Toute personne ayant eu un contact physique direct non protégé avec la peau lésée ou les fluides biologiques d’un cas probable ou confirmé symptomatique, quelles que soient les circonstances y compris rapport sexuel, actes de soin médical ou paramédical, ou partage d’ustensiles de toilettes, ou contact avec des textiles (vêtements, linge de bain, literie) ou de la vaisselle sale utilisés par le cas probable ou confirmé symptomatique.
- Toute personne ayant eu un contact non protégé à moins de 2 mètres pendant 3 heures (cumulées durant 24h) avec un cas probable ou confirmé symptomatique (ex. ami proche ou intime, partenaire sexuel habituel même en l’absence de rapports sexuels, personnes partageant le même lieu de vie sans lien intime, voisin pour un transport de longue durée, personnes partageant le même bureau, acte de soin ou d’hygiène, même classe scolaire, salle de TD universitaire, club de sport pour les sports de contacts, salles de sports…).
Le 16 août 2024. Le laboratoire produisant ce vaccin (Bavarian Nordic) a soumis des données à l'EMA pour étendre l'approbation du vaccin IMVANEX aux adolescents âgés de 12 à 17 ans.
Posologie
Dans les paragraphes qui suivent, les antécédents de vaccination contre la variole du singe ou contre les virus de la vaccine ont été ajoutés dans la version du RCP du 25 juillet 2022.
1. Primovaccination (personnes non précédemment vaccinées contre la variole, la variole du singe ou les virus de la vaccine)
Une première dose de 0,5 mL doit être administrée à une date donnée.
Une seconde dose de 0,5 mL doit être administrée au minimum 28 jours après la première dose.
Voir les rubriques "Mises en garde et précautions d'emploi" et "Pharmacodynamie".
2. Rappel de vaccination (personnes précédemment vaccinées contre la variole, la variole du singe ou les virus de la vaccine)
Il n’y a pas de données suffisantes pour déterminer le moment approprié pour les doses de rappel. Si une dose de rappel est jugée nécessaire, administrer une dose unique de 0,5 mL.
Voir les rubriques"Mises en garde et précautions d'emploi" et "Pharmacodynamie".
Tableau résumé des différents schémas de vaccination à effectuer chez les personnes éligibles à la vaccination en fonction des antécédents d’infection et de vaccination

MVA-BN = vaccin antivariolique de troisième génération (commercialisé sous le nom Imvanex en Europe et Jynneos aux États-Unis) ;
a Vaccin antivariolique reçu avant 1980 ;
* La dose de rappel doit être administrée à distance de la primovaccination et idéalement deux ans ou plus après la dernière dose. Les personnes éligibles à une dose de rappel ayant été primovaccinées en 2022 peuvent donc être revaccinées.
3. Populations particulières
Les patients immunodéprimés (par ex., personnes infectées par le VIH, patients sous traitement immunosuppresseur) qui ont été précédemment vaccinés contre la variole, la variole du singe ou les virus de la vaccine doivent recevoir deux doses de rappel. La seconde dose de rappel doit être administrée au moins 28 jours après la première dose de rappel.
4. Population pédiatrique
La sécurité et l’efficacité d’IMVANEX chez les enfants âgés de moins de 12 ans n’ont pas été établies.
Aucune donnée n’est disponible.
En cas de contact à risque
Vaccination dans les 4 jours après le contact à risque et au maximum 14 jours plus tard.
Schéma à deux doses espacées de 28 jours.
Personnes immunodéprimées : trois doses espacées de 28 jours.
En cas de tension d’approvisionnement des vaccins
La HAS recommande que la priorité soit donnée à la vaccination en post-exposition des personnes contacts à risque et estime que l’administration de la seconde dose pourra être différée de plusieurs semaines en cas de besoin. Cette recommandation est conforme au RCP, qui définit un intervalle minimal entre les doses.
Mode d'administration
L’injection du vaccin doit se faire par voie sous-cutanée, de préférence dans le haut du bras.
Pour les instructions concernant l’administration, voir rubrique "Manipulation".
La voie intradermique est temporairement autorisée car elle permet des économies de vaccin. La dose utilisée par voie sous-cutanée est de 0,5 mL. La dose utilisée par voie intradermique est égale à 1/5e de ce volume, soit 0,1 mL. Avis de l'ANSM :
- Les données cliniques disponibles montrent que l’injection d’une dose de 0,1 mL du vaccin MVA-BN (Imvanex/Jynneos) par voie intradermique (ID) est aussi immunogène qu’une dose de 0,5 mL par voie sous cutanée (SC). Néanmoins, les données de sécurité indiquent une moins bonne tolérance au site d’injection (intensité plus élevée et persistance plus longue des symptômes tels que des rougeurs, un gonflement et des démangeaisons, etc.) en comparaison à la voie sous-cutanée jusqu’à 6 mois post-injection chez plus d’un tiers des participants.
- Dans le cas d’approvisionnements limités en vaccins, la voie ID parait une alternative possible. Il semble néanmoins important d’encadrer sa mise en place (professionnels de santé expérimentés ou si nécessaire ayant bénéficié d’une formation).
- Des données supplémentaires sont nécessaires pour déterminer le nombre de vaccinations réalisables avec un flacon de 0,5 mL, en fonction du dispositif d’injection et en respectant la durée de conservation d’un flacon ouvert. Toutefois, les US CDC rappellent qu’une fois le flacon percé pour prélever la 1ère dose, le vaccin doit être utilisé dans les 8 heures et conservé au réfrigérateur entre chaque prélèvement. Si la quantité de vaccin restant dans le flacon ne permet pas d’obtenir une dose complète de 0,1 mL, le flacon et la solution résiduelle doivent être éliminés. Ces modalités d’utilisation paraissent pouvoir être suivies.
Ainsi, une utilisation d’Imvanex/Jynneos par voie ID à la posologie de 0,1 mL présente un rapport bénéfice/risque favorable et pourrait être justifiée dans le cas d’approvisionnements limités en vaccins. Dans ces circonstances, il est par exemple envisageable de proposer la 2ème dose par voie ID aux personnes ayant reçu une première dose par voie SC et qui ont manifesté pas ou peu de symptômes au site d’injection.
L’ANSM préconise d’utiliser la voie ID seulement chez les personnes âgées de plus de 18 ans et de ne pas utiliser la voie ID chez les femmes enceintes.
Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique "Composition" ou aux résidus présents à l’état de traces (protéines de poulet, benzonase, gentamicine et ciprofloxacine).
Mises en garde et précautions d'emploi
1. Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
2. Hypersensibilité et anaphylaxie
Comme pour tout vaccin injectable, un traitement médical approprié doit toujours être disponible immédiatement et une surveillance doit être effectuée pour le cas rare où surviendrait une réaction anaphylactique après administration du vaccin.
3. Maladies concomitantes
La vaccination doit être différée chez les personnes souffrant d’une maladie fébrile aiguë sévère ou d’une infection aiguë. La présence d’une infection mineure et/ou d’une fébricule ne doit pas entrainer le report de la vaccination.
4. Recommandations générales
IMVANEX ne doit pas être administré par injection intravasculaire.
5. Limites de l’efficacité du vaccin
L’efficacité protectrice d’IMVANEX contre la variole, la variole du singe et la maladie causée par le virus de la vaccine n’a pas été étudiée chez l’être humain, voir la rubrique "Pharmacodynamie".
Une réponse immunitaire protectrice peut ne pas être induite chez toutes les personnes vaccinées.
Il n’y a pas de données suffisantes pour déterminer le moment approprié pour les doses de rappel.
Une vaccination antérieure par IMVANEX peut modifier la réponse cutanée (« prise ») à l’administration ultérieure d’un vaccin antivariolique capable de se répliquer, avec pour conséquence une prise réduite ou absente, voir la rubrique "Pharmacodynamie".
6. Personnes atteintes de dermatite atopique
Les personnes atteintes de dermatite atopique ont développé davantage de symptômes locaux et généraux après la vaccination (voir la rubrique "Effets indésirables").
7. Personnes immunodéprimées
Des données ont été obtenues chez des patients infectés par le VIH avec une numération des lymphocytes CD4 ≥ 100 cellules/μl et ≤ 750 cellules/μl. Une réponse immunitaire plus faible a été observée chez les patients infectés par le VIH par rapport aux sujets sains (voir la rubrique "Pharmacodynamie"). Aucune donnée n’est disponible concernant la réponse immunitaire vis-à-vis d’IMVANEX chez les autres personnes immunodéprimées.
Deux doses d’IMVANEX administrées à 7 jours d’intervalle ont induit des réponses immunitaires plus faibles et une réactogénicité locale légèrement plus importante que deux doses administrées à 28 jours d’intervalle. Par conséquent, les intervalles entre les doses inférieurs à 28 jours doivent être évités.
8. Réactions liées à l’anxiété
Des réactions liées à l’anxiété, y compris des réactions vasovagales (syncope), une hyperventilation ou des réactions liées au stress, peuvent survenir lors de la vaccination sous la forme d’une réponse psychogène à l’injection via l’aiguille. Il est important que des mesures de précaution soient en place afin d’éviter toute blessure consécutive à un évanouissement.
9. Teneur en sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu’il est essentiellement « sans sodium ».
Interactions
Aucune étude d’interaction avec d’autres vaccins ou médicaments n’a été réalisée.
Par conséquent, l’administration concomitante d’IMVANEX et d’autres vaccins doit être évitée.
L’administration concomitante du vaccin et d’immunoglobulines, y compris le VIG (Vaccinia Immune Globulin), n’a pas été étudiée et doit être évitée.
Fertilité
Les études effectuées chez l’animal n’ont pas mis en évidence d’altération de la fertilité, ni chez les femelles ni chez les mâles.
Grossesse
Il existe des données limitées (moins de 300 grossesses) sur l’utilisation d’IMVANEX chez la femme enceinte. Les études effectuées chez l’animal n’ont pas mis en évidence d’effets délétères directs ou indirects sur la reproduction. Par mesure de précaution, il est préférable d’éviter l’utilisation d’IMVANEX pendant la grossesse.L’administration d’IMVANEX pendant la grossesse ne doit être envisagée que si les bénéfices potentiels sont supérieurs à tout risque potentiel pour la mère et le foetus.
Allaitement
On ne sait pas si IMVANEX est excrété dans le lait maternel.
Par mesure de précaution, il est préférable d’éviter l’utilisation d’IMVANEX pendant l’allaitement. L’administration d’IMVANEX pendant l’allaitement ne doit être envisagé que si les bénéfices potentiels sont supérieurs à tout risque potentiel pour la mère et le bébé.
Effets indésirables
1. Résumé des effets indésirables
1.1. Résumé du profil de sécurité
La sécurité d’IMVANEX a été évaluée lors de 20 essais cliniques au cours desquels 5 261 personnes non vaccinées par le virus de la vaccine ont reçu deux doses d’au moins 5 x 107 U. Inf. à quatre semaines d’intervalle et 534 personnes précédemment vaccinées par le virus de la vaccine et avec IMVANEX ont reçu une dose de rappel unique.
Les effets indésirables les plus fréquemment observés lors des essais cliniques étaient des réactions au site d’injection et des réactions systémiques couramment observées après une vaccination ; ces réactions ont été d’intensité légère à modérée et ont disparu sans traitement dans les sept jours suivant la vaccination.
Les fréquences des effets indésirables décrits après chaque dose de vaccin (1re, 2eou dose de rappel) ont été similaires.
1.2. Les effets indésirables
Les effets indésirables observés dans l’ensemble des essais cliniques sont classés par ordre de fréquence selon la convention suivante :
- Très fréquent (≥ 1/10)
- Fréquent (≥ 1/100, < 1/10)
- Peu fréquent (≥ 1/1 000, < 1/100)
- Rare (≥ 1/10 000, < 1/1 000)
- Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
Effets indésirables décrits lors des essais cliniques (n = 7 082 sujets) et dans le cadre de l’expérience post-autorisation avec IMVANEX
Infections et infestations
- Peu fréquent : rhinopharyngite, infection des voies respiratoires supérieures
- Rare : sinusite, conjonctivite, grippe
Affections hématologiques et du système lymphatique
- Peu fréquent : lymphadénopathie
Troubles du métabolisme et de la nutrition
- Fréquent : troubles de l'appétit
Affections psychiatriques
- Peu fréquent : troubles de sommeil
Affections du système nerveux
- Très fréquent : céphalées
- Peu fréquent : sensations vertigineuses, paresthésies
- Rare : migraine, neuropathie sensitive périphérique, somnolence
- Indéterminé : paralysie faciale périphérique aiguë (paralysie de Bell)
Affections de l'oreille et du labyrinthe
- Rare : vertiges
Affections cardiaques
- Rare : tachycardie
Affections respiratoires, thoraciques et médiastinales
- Peu fréquent : douleur pharyngolaryngée, rhinite, toux
- Rare : douleurs oro-pharyngées
Affections gastro- intestinales
- Très fréquent : nausées
- Peu fréquent : diarrhée, vomissement
- Rare : douleur abdominale, sécheresse buccale
Affections de la peau et du tissu sou-cutané
- Peu fréquent : éruption cutanée, prurit, dermatite
- Rare : urticaire, décoloration de la peau, ecchymose, hyperhidrose, sueurs nocturnes, nodule sous-cutané, œdème de Quincke
Affections musculo- squelettiques et systémiques
- Très fréquent : myalgies
- Fréquent : douleur dans l'extrémité, arthralgies
- Peu fréquent : raideur musculo-squelettique
- Rare : dorsalgie, douleur dans le cou, spasme musculaires, douleur musculo-squelettique, faiblesse musculaire
Troubles généraux et anomalies au site d’administration
- Très fréquent : douleur au site d’injection, érythème au site d’injection, gonflement au site d’injection, induration au site d’injection, prurit au site d’injection, fatigue
- Fréquent : frissons, nodule au site d’injection, décoloration au site d’injection, hématome au site d’injection, chaleur au site d’injection
- Peu fréquent : gonflement au niveau des aisselles, malaise, hémorragie au site d’injection, irritation au site d’injection, bouffées vasomotrices, douleur thoracique
- Rare : douleur axillaire, desquamation au site d’injection, inflammation au site d’injection, paresthésie au site d’injection, réaction au site d’injection, éruption cutanée au site d’injection, œdème périphérique, asthénie, anesthésie au site d’injection, sécheresse au site d’injection, altération de la mobilité au site d’injection, syndrome pseudo-grippal, vésicules au site d’injection
Investigations
- Fréquent : élévation de la température corporelle, pyrexie
- Peu fréquent : élévation de la troponine I, élévation des enzymes hépatiques, diminution de la numération leucocytaire, diminution du volume plaquettaire moyen
- Rare : élévation de la numération leucocytaire
Lésions, intoxications et complications liées aux procédures
- Rare : contusion
1.3. Personnes atteintes de dermatite atopique
Lors d’un essai clinique non contrôlé contre placebo ayant comparé la sécurité d’IMVANEX chez des personnes atteintes de dermatite atopique et chez des sujets sains, les personnes atteintes de dermatite atopique ont présenté un érythème (61,2 %) et un gonflement (52,2 %) au site d’injection à une fréquence plus élevée que chez les sujets sains (49,3 % et 40,8 %, respectivement). Les symptômes généraux suivants ont été signalés plus fréquemment chez les personnes atteintes de dermatite atopique que chez les sujets sains : céphalées (33,1 % contre 24,8 %), myalgies (31,8 % contre 22,3 %), frissons (10,7 % contre 3,8 %), nausées (11,9 % contre 6,8 %) et fatigue (21,4 % contre 14,4 %).
Lors des essais cliniques d’IMVANEX, 7 % des personnes atteintes de dermatite atopique ont présenté une poussée ou une aggravation de leur affection cutanée au cours de l’étude.
1.4. Éruption cutanée
IMVANEX peut provoquer des éruptions cutanées localisées ou plus étendues. Les éruptions cutanées après vaccination (cas associés observés chez 0,64 % des sujets) avec IMVANEX ont tendance à survenir dans les premiers jours qui suivent la vaccination, sont d’intensité légère à modérée et disparaissent généralement sans séquelles.
2. Effets sur l’aptitude à conduire des véhicules et à utiliser des machines
On ne dispose pas d’informations concernant l’effet d’IMVANEX sur l’aptitude à conduire des véhicules et à utiliser des machines. Cependant, certains des effets indésirables mentionnés à la rubrique "Effets indésirables" sont susceptibles d’affecter l’aptitude à conduire des véhicules et à utiliser des machines (par ex., sensations vertigineuses).
3. Surdosage
Aucun cas de surdosage n’a été décrit.
4. Déclaration des effets indésirables suspectés
Il est important de signaler les effets indésirables présumés après l'autorisation du médicament. Ce signalement permet de surveiller en permanence le rapport bénéfice/risque du vaccin. Les professionnels de santé sont invités à signaler tout effet indésirable présumé par le biais du système national de notification et à indiquer le numéro de lot si celui-ci est disponible.
Population pédiatrique
Adolescents âgés de 12 à 18 ans
Les données intermédiaires issues de l’étude DMID 22‑0020, qui est toujours en cours, semblent indiquer un profil de sécurité largement similaire chez les adolescents à celui observé chez les adultes. Au total, 315 adolescents ont été inclus dans l’étude. Les données recueillies jusqu’au jour 57 de
l’étude sont considérées comme propres. Plus de 99 % des participants ont reçu deux doses de vaccin. D’après la base de données actuelle, la réaction au site d’injection la plus fréquente a été la douleur au site d’injection (> 70 %) et les effets indésirables systémiques les plus fréquents ont été la fatigue
(> 50 %) et les céphalées (50 %).
Pharmacodynamie
Classe pharmacothérapeutique : Vaccin, autres vaccins antiviraux, Code ATC : J07BX
Données sur l'efficacité en vie réelle de ce vaccin contre le mpox.
L'efficacité vaccinale en vie réelle (encore appelée efficacité sur le terrain ou "effectiveness" en anglais) dépend de plusieurs facteurs (population concernée, notamment la proportion de personnes immunodéprimées, définition des cas, confirmation biologique ou non des cas, temps écoulé depuis la vaccination, étude cas-témoins ou de cohorte, efficacité après une seule dose ou après deux doses...).
Dans cette revue systématique et méta-analyse publiée en juin 2024 (Vaccine effectiveness of 3rd generation mpox vaccines against mpox and disease severity: A systematic review and meta-analysis), les auteurs ont constaté que 1 ou 2 doses du vaccin IMVANEX étaient très efficaces pour prévenir le mpox, avec une efficacité vaccinale (de 76 % (IC 95 % : 64-88 %) pour 1 dose et de 82 % (IC 95 % : 72-92 %) pour 2 doses.
Une étude de cohorte réalisée en France chez des personnes non immunodéprimées (Impact of vaccination with third generation modified vaccinia Ankara and sexual behaviour on mpox incidence in men who have sex with men: analysis among participants of the ANRS-174 DOXYVAC trial) montre une efficacité vaccinale de 99 % contre la maladie mpox.
Rappelons que les patients immunodéprimés doivent recevoir 2 doses de rappel (soit 3 doses au total).
1. Efficacité chez l’animal
Les études sur les primates non humains (PNH) ont démontré que la vaccination avec IMVANEX induisait une réponse immunitaire et une efficacité protectrice comparables à celles conférées par les vaccins antivarioliques classiques utilisés pour éradiquer la variole et protégeait les PNH contre la maladie sévère associée à l’épreuve d’inoculation létale du virus de la variole simienne. Comme dans le cas des vaccins antivarioliques classiques, une réduction significative de la mortalité et de la morbidité (charge virale, perte de poids, nombre de lésions varioliques, etc.) par rapport aux animaux témoins non vaccinés a été démontrée chez les PNH vaccinés avec IMVANEX.
Les études sur la souris ont démontré que la vaccination avec IMVANEX protégeait les souris contre le risque létal du virus de la vaccine réplicatif.
2. Immunogénicité
2.1. Taux de séroconversion à la vaccine chez les sujets sains et les populations particulières non vaccinés par le virus de la vaccine
Les personnes non vaccinées par le virus de la vaccine comprenaient des sujets sains, ainsi que des personnes infectées par le VIH et atteintes de dermatite atopique. Ils ont reçu 2 doses d’IMVANEX à 4 semaines d’intervalle. Les taux de séroconversion chez des personnes non vaccinées par le virus de la vaccine étaient définis sur la base de l’apparition de titres d’anticorps supérieurs ou égaux à la valeur seuil du test après administration de deux doses d’IMVANEX. Les taux de séroconversion déterminés par les tests ELISA et PRNT ont été les suivants :
Tableau 1 : taux de séroconversion déterminés par ELISA chez les sujets sains et les populations particulières non vaccinés par le virus de la vaccine
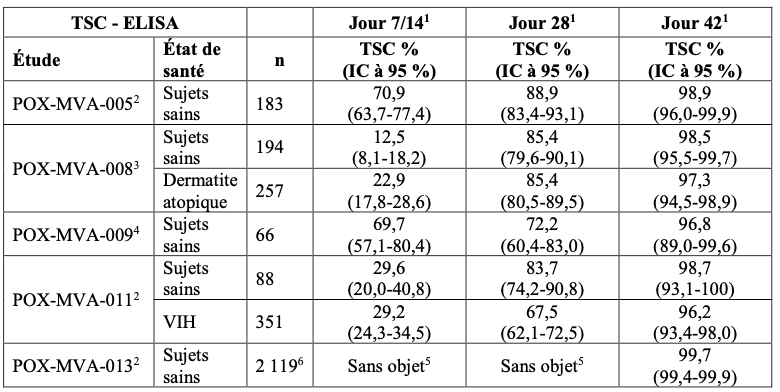

Tableau 2 : Taux de séroconversion déterminés par PRNT chez les sujets sains (incluant des adultes et des adolescents âgés de 12 à 17 ans) et les populations particulières non vaccinés par le virus de la vaccine
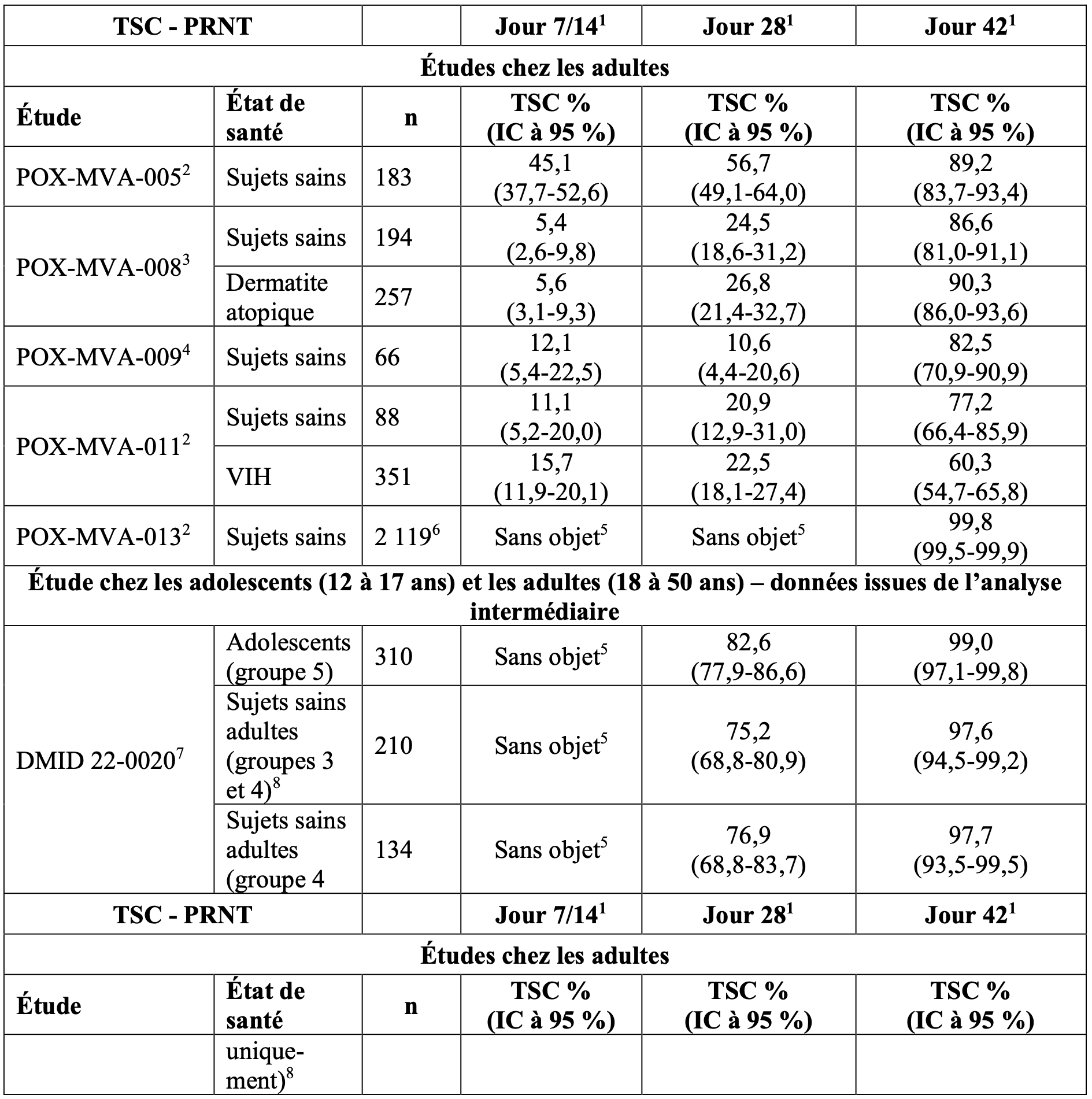
TSC = taux de séroconversion ;
PRNT = test de séroneutralisation par réduction des plages de lyse ;
ELISA = test immuno-enzymatique utilisant le virus de la vaccine modifié comme antigène ;
2 Analyse de l’Ensemble de la Population (FAS, Full Analysis Set) (pour l’étude POX-MVA-013 : analyse de l’immunogénicité) ;
3 Analyse per protocole (PP) ;
4 Taux de séropositivité ;
5 Aucun échantillon prélevé pour l’analyse de l’immunogénicité ;
6 Groupes 1-3 combinés.
7 Nombre de participants au sein de la population en ITTm ; 8 Les groupes 3 et 4 combinés ont été utilisés comme groupe comparateur lors de l’analyse primaire.
2.2. Taux de séroconversion à la vaccine chez les sujets sains et les populations particulières précédemment immunisées contre le virus de la vaccine
La séroconversion chez les personnes précédemment immunisées contre le virus de la vaccine était définie sur la base d’une augmentation d’un facteur deux au moins des titres initiaux après une vaccination unique par IMVANEX.
Tableau 3 : taux de séroconversion déterminés par ELISA chez les sujets sains et les populations particulières précédemment immunisés contre le virus de la vaccine
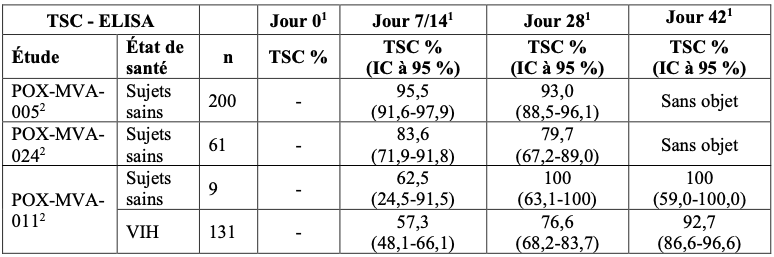

Tableau 4 : tauxde séroconversion déterminés par PRNT chez les sujets sains et les populations particulières précédemment immunisés contre le virus de la vaccine
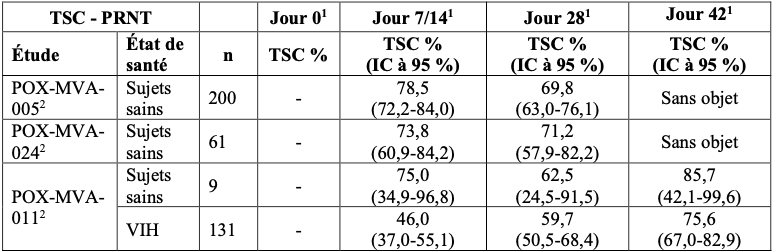

TSC = taux de séroconversion ;
2 Analyse de l’Ensemble de la Population (FAS) ;
PRNT = test de séroneutralisation par réduction des plages de lyse ;
ELISA = test immuno-enzymatique utilisant le virus de la vaccine modifié comme antigène.
3. Immunogénicité à long terme à la vaccine chez l’être humain
Des données limitées sur l’immunogénicité à long terme couvrant une période de 24 mois après la primovaccination avec IMVANEX chez les personnes non vaccinées par le virus de la vaccine sont actuellement disponibles, comme spécifié ci-dessous :
Tableau 5 : taux de séroconversion déterminés par ELISA et PRNT chez les sujets sains non vaccinés par le virus de la vaccine sur une période de 24 mois
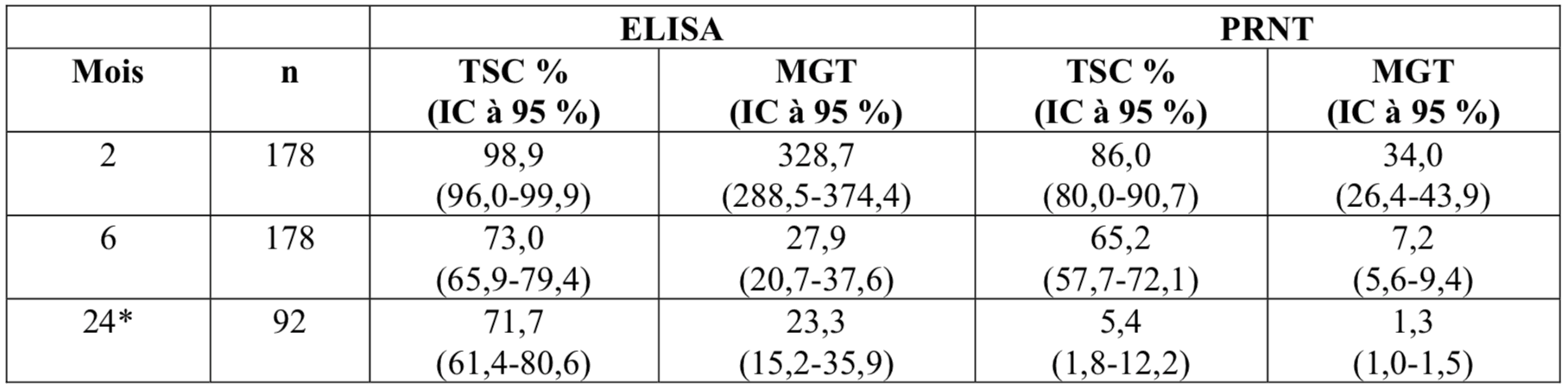

MGT= moyenne géométrique du titre ;
n = nombre de sujets dans le groupe expérimental concerné ;
PRNT = plaque reduction neutralization test (test de neutralisation par réduction du nombre de plaques) ;
TSC = taux de séroconversion ;
* Représente le taux de séropositivité.
4. Dose de rappel
Deux études cliniques ont montré qu’IMVANEX est à même de stimuler une réponse immunologique à la vaccine en présence d’une mémoire immunitaire préexistante induite soit par un vaccin antivariolique homologué administré longtemps auparavant, soit deux ans après IMVANEX.
Tableau 6 : taux de séroconversion déterminés par ELISA et PRNT après une dose de rappel
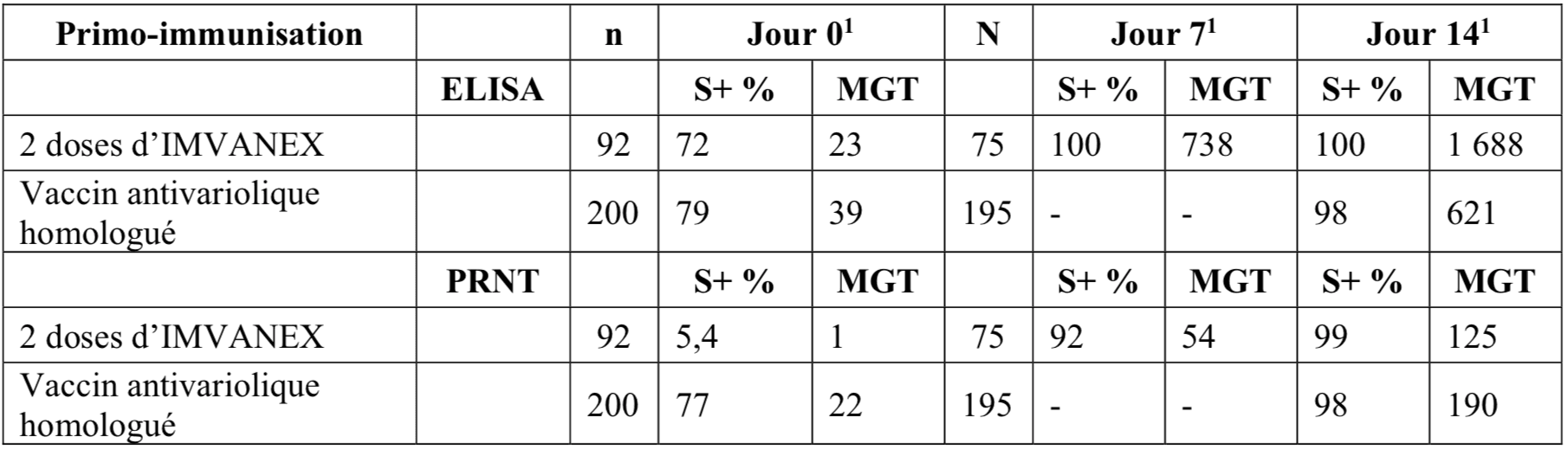

n = nombre de sujets dans le groupe expérimental concerné ;
ELISA = test immuno-enzymatique utilisant le virus de la vaccine modifié comme antigène ;
PRNT = plaque reduction neutralization test(test de neutralisation par réduction du nombre de plaques) ;
S+ = taux de séropositivité MGT= moyenne géométrique du titre.
5. Immunogénicité et atténuation de la prise du vaccin ACAM2000 chez des sujets sains
IMVANEX a été comparé au vaccin ACAM2000 (un vaccin antivariolique vivant atténué de « deuxième génération » produit sur culture cellulaire et bénéficiant d’une AMM aux États-Unis) dans le cadre d’un essai clinique de non-infériorité randomisé, en ouvert, chez des adultes en bonne santé (personnel militaire américain) âgés de 18 à 42 ans qui n’avaient jamais reçu de vaccin antivariolique (étude POX-MVA-006).
Au total, 433 sujets ont été randomisés selon un ratio de 1/1 en vue de recevoir soit deux doses d’IMVANEX suivies d’une dose unique d’ACAM2000 à quatre semaines d’intervalle, soit une dose unique d’ACAM2000. Le vaccin ACAM2000 a été administré par scarification.
Le premier critère d’évaluation primaire conjoint portait sur la comparaison des réponses en anticorps neutralisants spécifiques à la vaccine lors des visites au pic de concentration (au jour 42 après la première vaccination pour IMVANEX chez les sujets ayant reçu deux doses conformément au calendrier de vaccination standard et au jour 28 pour le vaccin ACAM2000). IMVANEX a induit un pic de la moyenne géométrique du titre (MGT) des anticorps neutralisants de 153,5 (n = 185 ; IC à 95 % : 134,3 ; 175,6), soit une valeur non inférieure à la MGT de 79,3 (n = 186 ; IC à 95 % : 67,1 ; 93,8) obtenue après l’administration d’ACAM2000 par scarification.
Le second critère d’évaluation primaire conjoint a évalué si la vaccination par IMVANEX (n = 165) avant administration d’ACAM2000 entraînait une atténuation de la réaction cutanée à ACAM2000 (n = 161) telle que mesurée d’après la surface de lésion maximale en mm. Au jour 13-15, la surface de lésion maximale médiane a été de 75 mm2 (IC à 95 % : 69,0 ; 85,0) chez les sujets ayant reçu le vaccin ACAM2000, et de 0,0 (IC à 95 % : 0,0 ; 2,0) chez ceux ayant reçu IMVANEX.
Efficacité du vaccin
Dans les études observationnelles en vie réelle menées auprès de personnes éligibles à la vaccination (conformément aux recommandations locales), l’efficacité du vaccin contre la variole du singe a été démontrée au moins 14 jours après la vaccinationa, avec des estimations ajustées de l’efficacité vaccinale allant de 35 % (IC à 95 %, -2-59) à 89 % (IC à 95 %, 76-95) après une dose d’IMVANEX et de 66 % (IC à 95 %, 47-78) à 90 % (IC à 95 %, 86-92) après deux doses d’IMVANEX.
Tableau 7 : Efficacité du vaccin au moins 14 jours après la vaccination a
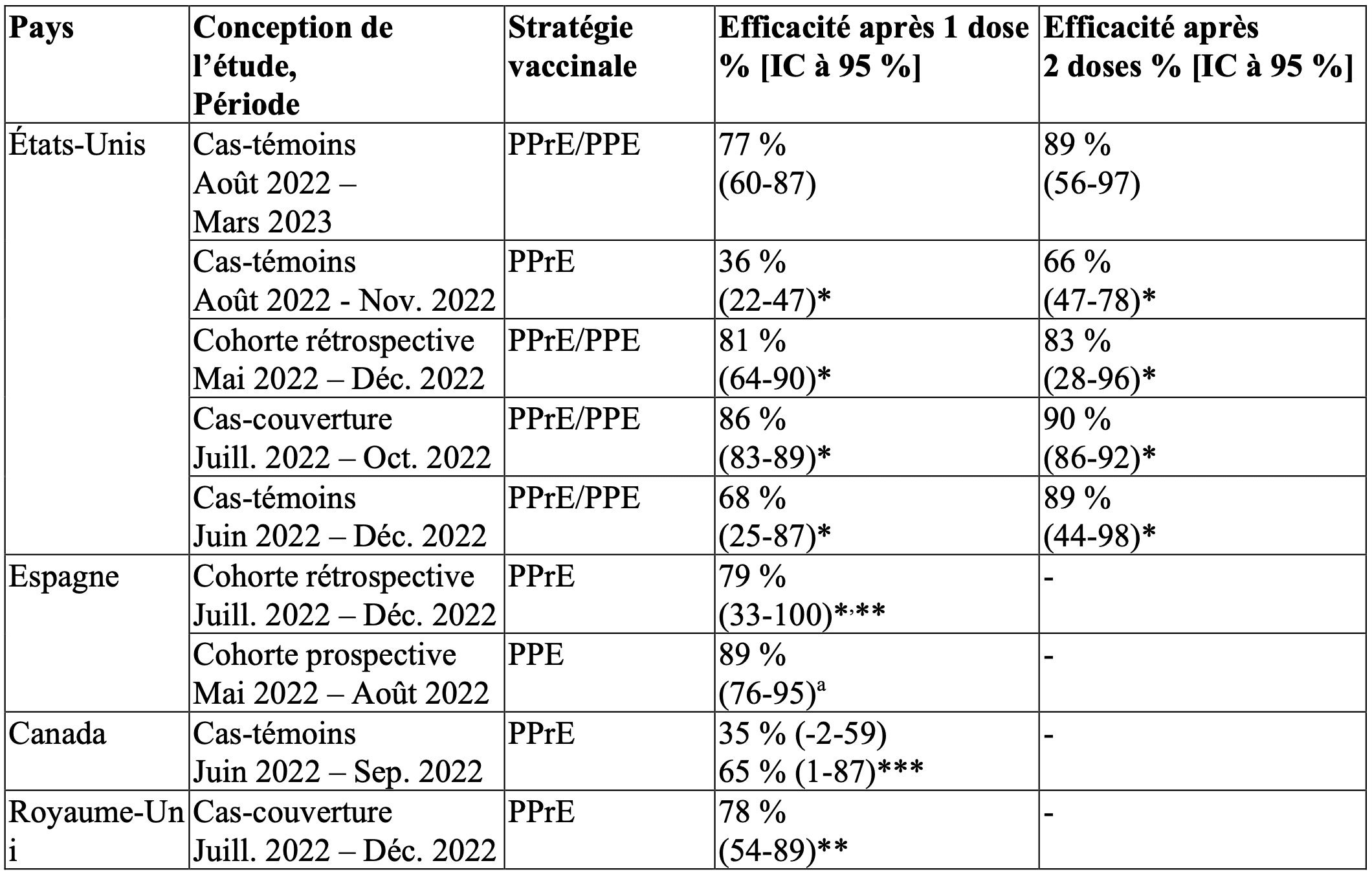
* Couvre à la fois les administrations sous-cutanées et intradermiques.
** Efficacité vaccinale brute.
*** Basé sur des données individuelles complétées par des réponses à des questionnaires sur les comportements à risque.
a PPE administrée ≤ 14 jours après l’exposition.
Impact sur les hospitalisations
Dans une étude de surveillance menée de mai 2022 à mai 2023 aux États-Unis, il a été démontré qu’IMVANEX réduisait les risques d’hospitalisation liés à la variole du singe. Par rapport aux patients atteints de la variole du singe non vaccinés, les probabilités d’hospitalisation étaient de 0,27 (IC à 95 %, 0,08-0,65) après une dose d’IMVANEX, et de 0,20 (IC à 95 %, 0,01-0,90) après deux doses d’IMVANEX. La réduction estimée du risque relatif était de 73 % après une dose d’IMVANEX et de 80 % après deux doses d’IMVANEX.
6. Population pédiatrique
L’Agence européenne des médicaments a différé l’obligation de soumettre les résultats d’études réalisées avec IMVANEX dans un ou plusieurs sous-groupes de la population pédiatrique de la population pédiatrique pour la prévention de la variole, de la variole du singe et la maladie causée par le virus de la vaccine par immunisation active contre l’infection par le virus de la variole, le virus de la variole du singe et l’affection due à l’infection par le virus de la vaccine et la maladie de la vaccine (voir rubrique "Posologie" pour les informations concernant l’usage pédiatrique).
Une étude chez les adolescents (DMID 22-00207) est actuellement en cours et les données d’immunogénicité jusqu’au jour 43 de l’étude (14 jours après la deuxième dose) sont déjà disponibles. Les résultats obtenus pour le critère d’évaluation primaire montrent une non-infériorité de la réponse en anticorps chez les adolescents par rapport aux adultes sur la base du test de neutralisation spécifique à la vaccine.
Tableau 8 : Test de l’hypothèse primaire par PRNT spécifique au virus de la vaccine, population en ITT (m)
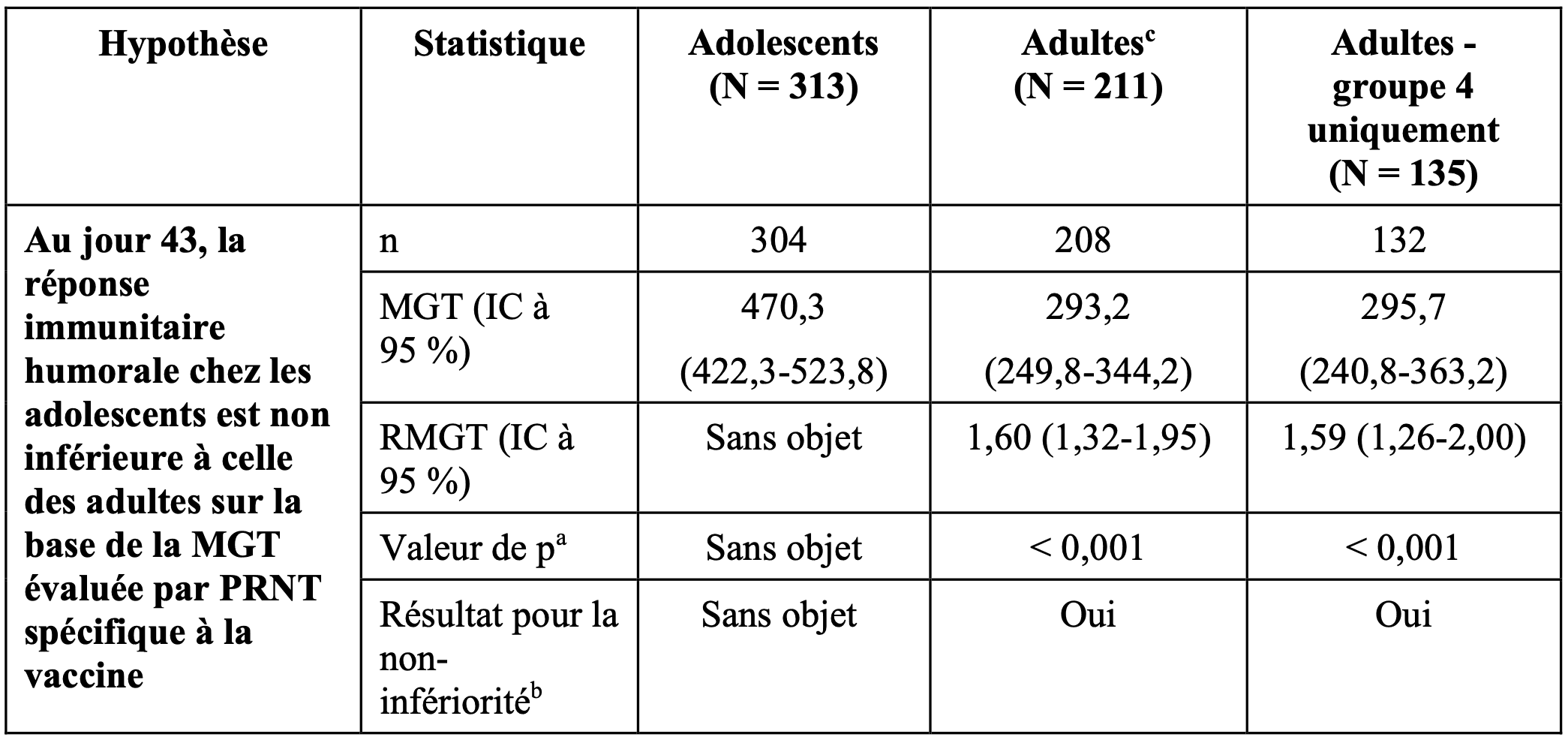
RMGT = ratio des moyennes géométriques des titres entre les adolescents et les adultes ;
IC = intervalle de confiance, calculé suivant la loi de distribution t de Student pour la MGT et le test t de Welch-Satterthwaite pour le RMGT.
a Test t à deux échantillons de variance inégale, avec marge de non-infériorité (NI) de 0,67 et taux d’erreur de type I bilatéral de 0,05 pour le test de l’hypothèse nulle selon laquelle la réponse immunitaire humorale chez les adolescents sera non inférieure à celle des adultes.
b Si la borne inférieure de l’IC à 95 % du RMGT est supérieure ou égale à 0,67 (NI = 0,174 log10) avant arrondi, le résultat
est « Oui ».
c Les groupes 3 et 4 combinés ont été utilisés comme groupe comparateur lors de l’analyse primaire. Les participants du
groupe 3 ont été exclus pour une analyse de sensibilité.
7. Circonstances exceptionnelles
Une autorisation de mise sur le marché « sous circonstances exceptionnelles » a été délivrée pour ce médicament.
Cela signifie qu’en raison de la rareté de cette maladie, il n’a pas été possible d’obtenir des informations complètes concernant ce médicament.
L’Agence européenne du médicament réévaluera chaque année toute nouvelle information qui pourrait être disponible, et, si nécessaire, ce RCP sera mis à jour.
Conservation
1. Durée de conservation
- 3 ans à -20 °C ± 5 °C
- 5 ans à -50 °C ± 10 °C
- 9 ans à -80 °C ± 10 °C
Après décongélation, le vaccin peut être conservé à l’obscurité entre 2°C et 8°C pendant 2 mois au maximum avant l’utilisation, dans les limites de la durée de conservation autorisée.
Ne pas recongeler un flacon qui a été décongelé.
2. Précautions particulières de conservation
A conserver au congélateur (à -20 °C ± 5 °C ou à -50 °C ± 10 °C ou à -80 °C ± 10 °C). La date de péremption dépend de la température de conservation.
Le vaccin peut être conservé à court terme au réfrigérateur entre 2°C et 8°C pendant 2 mois au maximum avant l’utilisation, dans les limites de la durée de conservation autorisée.
A conserver dans l’emballage extérieur d’origine à l’abri de la lumière.
Des durées de stockage différentes sont autorisées pour les différents marchés. Par exemple, la FDA (Food and Drug Administration, Etats-Unis), a approuvé un stockage de 24 semaines à 2-8 °C après un stockage préalable à -50 °C (au lieu de 2 mois après une décongélation suivant une congélation à -20 °C). Il n'existe pas de données concernant la durée de conservation de IMVANEX ou JYNNEOS à 2-8°C, en cas de décongélation suivant un stockage à -80 °C.
Cependant, lorsque la température de conservation est plus basse, l'agitation moléculaire est plus faible et les produits, notamment les produits biologiques vivants, sont mieux conservés. On peut donc présumer qu'après une décongélation suivant une conservation à -80 °C, le vaccin peut être conservé pendant au moins 2 mois entre 2 °C et 8 °C.
Manipulation
Le flacon doit avoir atteint une température comprise entre 8°C et 25°C avant utilisation. Tourner délicatement le flacon pendant au moins 30 secondes avant utilisation.
Après décongélation, IMVANEX est une suspension de couleur jaune pâle à blanche, transparente à laiteuse. Elle peut contenir des floculats jaune pâle à blancs.
La suspension doit être inspectée visuellement pour mettre en évidence la présence de particules étrangères et un changement de coloration avant utilisation. Si le flacon est endommagé ou si la présence de particules étrangères et/ou une modification de l’aspect physique sont observées, éliminer le vaccin.
Prélever une dose de 0,5 mL dans une seringue pour injection.
Chaque flacon est à usage unique.
L'administration du vaccin doit être consignée par le médecin sur le carnet de vaccination ou de santé avec le numéro de lot. Il peut aussi être inscrit par le patient ou son médecin sur un carnet de vaccination numérique (version grand public ou professionnelle).
Tout vaccin non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Autres informations
Données de sécurité préclinique
Les données non cliniques issues des études de toxicologie en administration répétée, tolérance locale, fertilité chez les femelles, toxicité embryo-fœtale et postnatale n’ont pas révélé de risque particulier pour l’homme.