ZOSTAVAX
Laboratoire : Merck
Arrêt de commercialisation depuis le mois de juin 2024. Les stocks existants sont maintenus dans les circuits de distribution jusqu'à la date de péremption du dernier lot français distribué (lot X026375, péremption 31/01/2025). Le vaccin Shingrix est recommandé préférentiellement à ce vaccin.
Description
Vaccin vivant atténué contre le zona.
Forme et Présentation
ZOSTAVAX poudre et solvant pour suspension injectable.
ZOSTAVAX poudre et solvant pour suspension injectable en seringue préremplie.
Poudre et solvant pour suspension injectable.
La poudre est compacte et cristalline, blanche à blanc cassé.
Le solvant est un liquide clair, incolore.
Nature et contenu de l'emballage extérieur
ZOSTAVAX avec un solvant pour reconstitution fourni en flacon
- Poudre en flacon (verre) avec un bouchon (caoutchouc butyl), muni d’un capuchon amovible (aluminium) et solvant en flacon (verre) avec un bouchon (caoutchouc chlorobutyl) muni d’un capuchon amovible (aluminium).
Boîtes de 1 ou 10.
ZOSTAVAX avec un solvant pour reconstitution fourni en seringue préremplie
- Poudre en flacon (verre) muni d’un bouchon (caoutchouc butyl), et d’un capuchon amovible (aluminium) et solvant en seringue préremplie (verre) munie d’un bouchon piston (caoutchouc chlorobutyl) et protège-embout (caoutchouc styrène-butadiène) avec une ou deux aiguilles séparées.
Boîtes de 1, 10 ou 20. - Poudre en flacon (verre) muni d’un bouchon (caoutchouc butyl), et d’un capuchon amovible (aluminium) et solvant en seringue préremplie de (verre) munie d’un bouchon piston (caoutchouc chlorobutyl) et protège-embout (caoutchouc styrène-butadiène) sans aiguille.
Boîtes de 1, 10 ou 20.
Toutes les présentations peuvent ne pas être commercialisées.
Composition
Une dose (0,65 mL) contient après reconstitution :
1. Antigènes
- Virus varicelle-zona *, souche Oka/Merck, (vivant, atténué) - Pas moins de 19.400 UFP **.
** UFP = Unités formant plages.
2. Excipients
Poudre
- Saccharose
- Gélatine hydrolysée
- Chlorure de sodium *
- Phosphate de potassium dihydrogéné
- Chlorure de potassium **
- L-Glutamate monosodique monohydraté
- Phosphate de sodium
- Hydroxyde de sodium (pour ajuster le pH)
- Néomycine (traces)
- Urée
** Ce médicament contient moins de 1 mmol de potassium (39 milligrammes) par dose, c’est-à-dire qu’il est essentiellement « sans potassium ».
Solvant
- Eau pour préparations injectables
Ce vaccin peut contenir des traces de néomycine.
Indications
ZOSTAVAX est indiqué pour la prévention du zona et des douleurs post-zostériennes (NPZ).
ZOSTAVAX est indiqué pour la vaccination des sujets de 50 ans et plus.
Pris en charge par l'assurance maladie dans le cas suivant : prévention du zona et des douleurs postzostériennes des personnes âgées de 65 à 74 ans révolus.
Référence : arrêté du 5 juin 2015.
Posologie
Les sujets doivent recevoir une dose (0.65 mL).
La nécessité d’une dose de rappel n’est pas connue. Voir rubrique "Effets indésirables" et "Pharmacodynamie".
Population pédiatrique
La tolérance et l'efficacité de Zostavax chez les enfants et les adolescents n'ont pas été établies. Aucune donnée n'est disponible.
Il n'y a pas d'utilisation pertinente de Zostavax chez les enfants et adolescents pour la prévention primaire de la varicelle.
Mode d'administration
Le vaccin peut être injecté par voie sous-cutanée (SC) ou par voie intramusculaire (IM), de préférence dans la région deltoïdienne ( voir rubriques "Effets indésirables" et "Pharmacodynamie").
Le vaccin doit être administré par voie sous-cutanée chez les patients ayant une thrombocytopénie sévère ou un trouble de la coagulation ( voir rubrique "Mises en garde et précautions d'emploi").
Le vaccin ne doit en aucun cas être injecté par voie intravasculaire.
Pour les précautions à prendre avant la manipulation ou l'administration du médicament, voir rubrique "Manipulations".
Pour les instructions de reconstitution du médicament avant administration, voir rubrique "Manipulations".
Contre-indications
Antécédents d'hypersensibilité à la substance active, à l’un des excipients (voir rubrique "Composition") ou aux résidus présents à l’état de traces, comme la néomycine (voir rubriques "Mises en garde et précautions d’emploi" et la rubrique "Composition").
Immunodéficience primaire ou acquise due à des maladies comme : les leucémies aiguës et chroniques, les lymphomes, les autres affections de la moelle osseuse ou du système lymphatique, l’immunodéficience due au VIH/SIDA (voir rubriques "Mises en garde et précautions d’emploi", "Effets indésirable" et "Pharmacodynamie") ; les déficits de l’immunité cellulaire.
Traitement immunosuppresseur (y compris les fortes doses de corticostéroïdes) (voir rubriques "Mises en garde et précautions d’emploi" et "Effets indésirable") ; cependant, ZOSTAVAX n’est pas contre-indiqué chez les sujets recevant des corticostéroïdes par voie locale ou en inhalation ou des corticostéroïdes par voie parentérale à faible dose ou chez des patients recevant des corticostéroïdes en traitement substitutif, comme par exemple pour une insuffisance surrénale (voir rubriques "Effets indésirable" et "Pharmacodynamie").
Tuberculose active non traitée.
Grossesse. De plus, la grossesse doit être évitée dans le mois suivant la vaccination (voir rubriques "Grossesse", "Allaitement").
Mises en garde et précautions d'emploi
1. Traçabilité
Afin d’améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Un traitement médical approprié doit être disponible immédiatement et une surveillance doit être effectuée dans les rares cas où une réaction anaphylactique/anaphylactoïde surviendrait après l'administration du vaccin, en raison de possibles réactions d’hypersensibilité dues non seulement à la substance active mais aussi aux excipients et aux résidus (ex. : la néomycine) présents à l’état de traces dans le vaccin (voir les rubriques "Contre-indications", "Effets indésirable" et "Composition").
L’allergie à la néomycine se traduit généralement par une dermatite de contact. Cependant, un antécédent de dermatite de contact à la néomycine n’est pas une contre-indication aux vaccins à virus vivants.
ZOSTAVAX est un vaccin vivant atténué contre le virus varicelle-zona et son administration peut conduire à une infection disséminée chez les sujets immunodéprimés ou immunodéficients. Les patients qui ont déjà reçu un traitement immunosuppresseur doivent faire l'objet d'une évaluation attentive afin de vérifier la reconstitution de leur système immunitaire avant de leur administrer Zostavax (voir rubrique "Contre-indications").
La tolérance et l’efficacité de ZOSTAVAX n’ont pas été établies chez les adultes infectés par le VIH avec ou sans immunodépression avérée (voir rubrique "Contre-indications"). Cependant, une étude de tolérance et d'immunogénicité de phase II chez des adultes infectés par le VIH présentant une fonction immunitaire conservée (nombre de cellules T CD 4 + ≥ 200 cellules / µL) a été réalisée (voir rubriques "Effets indésirable" et "Pharmacodynamie").
Ce vaccin doit être administré par voie sous-cutanée chez les sujets ayant une thrombocytopénie sévère ou un trouble de la coagulation, en raison de l'apparition possible d'un saignement chez ces sujets suite à une injection par voie intramusculaire.
ZOSTAVAX n’est pas indiqué pour le traitement du zona ou des NPZ.
La vaccination doit être différée chez les sujets souffrant d'une maladie fébrile aiguë ou d'une infection modérée à sévère.
Comme pour tous les vaccins, la vaccination avec ZOSTAVAX peut ne pas protéger tous les sujets vaccinés. Voir rubrique "Pharmacodynamie".
2. Transmission
Dans les études cliniques faites avec ZOSTAVAX, aucun cas de transmission du virus vaccinal n’a été rapporté. Cependant, l'expérience acquise suite à la mise sur le marché des vaccins varicelleux suggère que la transmission du virus vaccinal entre des sujets vaccinés développant une éruption de type varicelle et des sujets contact « réceptifs » [par exemple, de jeunes enfants « réceptifs» au virus varicelle zona (VZV, Varicella Zoster Virus)] peut survenir dans de rares cas. La transmission du virus vaccinal par un individu vacciné contre la varicelle qui ne développe pas d'éruption de type varicelle a été aussi rapportée. Ceci est un risque théorique de la vaccination par ZOSTAVAX. Le risque de transmettre le virus vaccinal atténué d'un vacciné à un contact « réceptif » doit être évalué par rapport au risque de développer un zona naturel et de transmettre potentiellement le VZV sauvage à un contact « réceptif ».
Interactions
ZOSTAVAX peut être administré en même temps que le vaccin grippal inactivé en 2 injections distinctes réalisées en des sites différents (voir rubrique "Pharmacodynamie").
L’utilisation concomitante de ZOSTAVAX et d’un vaccin pneumococcique polyosidique comportant 23 valences a conduit à une diminution de l’immunogénicité du ZOSTAVAX au cours d'une petite étude clinique. Toutefois, les données recueillies lors d’une vaste étude observationelle n’ont pas révélé de risque accru de zona après l’administration concomitante des deux vaccins.
Il n’y a pas actuellement de données sur l’administration concomitante avec d’autres vaccins.
L’administration concomitante de ZOSTAVAX avec des traitements anti-viraux connus pour être efficaces contre le VZV n’a pas été évaluée.
Fertilité
Zostavax n'a pas été évalué dans des études de fécondité.
Grossesse
Il n'existe pas de données sur l'utilisation de ZOSTAVAX chez les femmes enceintes. les études traditionnelles non cliniques sont insuffisantes en ce qui concerne la toxicité sur la reproduction. Cependant, l'infection naturelle par le virus varicelle-zona est connu pour avoir parfois des effets néfastes sur le foetus. l'administration de ZOSTAVAX n'est pas recommandé aux femmes enceintes. Dans tous les cas, la grossesse doit être évitée pendant le mois suivant la vaccination (voir rubrique "Contre-indications").
Allaitement
On ne sait pas si le Virus Varicelle Zona est excrété dans le lait maternel. Un risque pour les nouveau-nés/nourrissons ne peut être exclu. La décision doit être prise soit d'interrompre l'allaitement, soit de ne pas administrer ZOSTAVAX, en tenant compte du bénéfice de l'allaitement pour l'enfant et du bénéfice de la vaccination pour la femme.
Effets indésirables
1. Résumé des effets indésirables
1.1. Résumé du profil de tolérance
Les effets indésirables les plus fréquemment rapportés dans les essais cliniques ont été des réactions au site d'injection. Les effets indésirables systémiques les plus fréquents ont été des céphalées et des douleurs des extrémités. La plupart de ces effets indésirables locaux et systémiques ont été signalés comme étant de faible intensité. Les effets indésirables graves liés au vaccin ont été rapportés chez 0.01 % des sujets vaccinés par ZOSTAVAX et des sujets ayant reçu le placebo.
Des données provenant d'une étude clinique (n=368) ont démontré que l'actuelle formulation réfrigérée possède un profil de tolérance comparable à celui de la formulation congelée.
1.2. Résumé des événement indésirables
Lors des essais cliniques, la tolérance générale de ZOSTAVAX a été évaluée chez plus de 57 000 adultes vaccinés avec ZOSTAVAX.
La liste 1 présente les réactions locales au site d’injection du vaccin et les effets indésirables généraux rapportés avec une fréquence significativement plus élevée dans le groupe vacciné que dans le groupe placebo dans les 42 jours suivant la vaccination dans l'étude d'efficacité et de tolérance de ZOSTAVAX (ZEST : ZOSTAVAX Efficacy and Safety Trial) et dans le sous-groupe de surveillance des événements indésirables de l'étude de prévention du zona (SPS : Shingles Prevention Study).
Les autres effets indésirables, rapportés spontanément par la surveillance post-commercialisation, sont également Liste 1. Comme ces évènements sont rapportés de façon volontaire à partir d'une population de taille incertaine, il n'est pas possible d'estimer de manière fiable leur fréquence ni d'établir un lien de cause à effet avec la vaccination. Par conséquent, les fréquences de ces effets indésirables ont été estimées sur la base des effets indésirables rapportés dans les études SPS et ZEST (indépendamment du lien de causalité attribué par l'investigateur).
Les effets indésirables sont classés par fréquence en utilisant la convention suivante :
- très fréquent (≥ 1/10) ;
- fréquent (≥ 1/100, < 1/10) ;
- peu fréquent (≥ 1/1 000, < 1/100) ;
- rare (≥ 1/10 000, < 1/1 000) ;
- très rare (< 1/10 000).
Liste 1 : événements indésirables rapportés pendant les études cliniques et après commercialisation
Infections et infestations
- Très rare : varicelle, Herpes zona (souche vaccinale).
Affections hématologiques et du système lymphatique
- Peu fréquent : lymphadénopathie (cervicale, axillaire).
Affections du système immunitaire
- Rare : réactions d'hypersensibilité incluant des réactions anaphylactiques.
Affections du système nerveux
- Fréquent : céphalées 1.
Affections oculaires
- Très rare : rétinite nécrosante (patients sous traitement immunosuppresseur).
Affections Gastro-intestinales
- Peu fréquent : nausées.
Affections de la peau et du tissu sous-cutané
- Fréquent : éruption cutanée.
Affections musculo squelettiques et systémiques
- Fréquent : arthralgies, myalgies, douleurs des extrémités 1.
Troubles généraux et anomalies au site d'administration
- Très fréquent : site d'injection : érythème 1,2, douleur/sensibilité au toucher 1,2, à la pression 1,2, prurit 1,2, gonflement 1,2.
- Fréquent : site d'injection : induration 1, hématome 1, chaleur 1, éruption cutanée et Fièvre.
- Rare : urticaire au site d'injection.
2 Effets indésirables rapportés dans les 5 jours suivant la vaccination.
1.3. Description des effets indésirables rapportés
Réaction au site d'injection
Les effets indésirables au site d'injection liés à la vaccination étaient significativement plus fréquents chez les sukets vaccinés par ZOSTAVAX que chez les sujets ayant reçu le placebo. Dans l'étude SPS, l'incidence globale des effets indésirables au site d'injection liés au vaccin étaient de 48 % pour ZOSTAVAX et de 17 % pour le placebo chez les sujets de 60 ans et plus.
Dans l'étude ZEST, l’incidence globale des effets indésirables au site d'injection liés au vaccin était de 63,9 % pour ZOSTAVAX et de 14,4 % pour le placebo chez les sujets de 50 à 59 ans. La plupart de ces effets indésirables ont été signalés comme étant de faible intensité.
Dans d'autres études cliniques évaluant ZOSTAVAX chez les sujets de 50 ans ou plus, y compris dans une étude de coadministration avec le vaccin grippal inactivé, un taux plus élevé d'effets indésirables d'intensité légère à modérée au site d'injection a été rapporté chez les sujets âgés de 50 à 59 ans par rapport aux sujets âgés de 60 ans et plus (voir rubrique "Pharmacodynamie").
ZOSTAVAX a été administré soit par voie sous-cutanée (SC) soit par voie intramusculaire (IM) chez des sujets de 50 ans ou plus (voir rubrique "Pharmacodynamie"). Le profil général de tolérance des voies SC et IM était globalement comparable, mais les effets indésirables au site d'injection étaient significativement moins fréquents dans le groupe IM (34 %) comparé au groupe SC (64 %).
Zona / éruptions de type zona et Varicelle / éruptions de type varicelle dans les essais cliniques
Dans les essais cliniques, le nombre de zona / éruption de type zona dans les 42 jours suivant la vaccination était faible dans les deux groupes ZOSTAVAX et placebo. La majorité des éruptions cutanées a été classée comme légère à modérée ; aucune complication de ces éruption n'a été observée dans le cadre clinique. La plupart des éruptions rapportées qui étaient VZV positives par analyse PCR a été associée à la souche sauvage VZV.
Dans les études SPS et ZEST, le nombre de sujets ayant signalé un zona / une éruption de type zona était inférieur à 0,2 % pour les groupes ZOSTAVAX et placebo, sans différence significative observée entre les deux groupes. Le nombre de sujets ayant signalé une varicelle / éruption de type varicelle était inférieur à 0,7 % pour les groupes ZOSTAVAX et placebo .
La souche Oka / Merck du VZV n'a été détectée dans aucun des échantillons des études SPS ou ZEST. Le VZV a été détecté dans un des échantillons (0,01 %) provenant d'un sujet ayant reçu ZOSTAVAX et ayant signalé une varicelle / éruption de type varicelle ; cependant, la souche du virus (souche sauvage ou souche Oka / Merck) n'a pas pu être déterminée. Dans tous les autres essais cliniques, la souche Oka / Merck a été identifiée par analyse PCR à partir des échantillons de lésions de deux sujets seulement qui ont signalé des éruptions de type varicelle (ayant débuté le jour 8 et le jour 17).
1.4. Populations particulières
Adultes ayant un antécédent de zona avant la vaccination
ZOSTAVAX a été administré à des sujets de 50 ans ou plus avec un antécédent de zona avant la vaccination (voir la rubrique "Pharmacodynamie"). Le profil de tolérance a été globalement comparable à celui observé au cours du suivi du Sous-Groupe de surveillance des événements indésirables de la SPS.
Adultes sous traitement d'entretien ou chronique par corticoïdes par voie systémique
Chez les sujets de 60 ans ou plus recevant un traitement d'entretien ou chronique par corticostéroïdes par voie systémique à une dose quotidienne équivalente de 5 à 20 mg de prednisone, depuis au moins 2 semaines avant l'inclusion et poursuivi au moins 6 semaines après la vaccination, le profil de tolérance a été globalement comparable à celui observé au cours du suivi du sous-groupe de surveillance des événements indésirables de l'étude SPS (voir les rubriques "Contre-indications" et "Pharmacodynamie").
Adultes infectés par le VIH ayant une fonction immunitaire conservée
Dans une étude clinique, ZOSTAVAX a été administré à des adultes infectés par le VIH (âgés de 18 ans et plus, nombre de lymphocytes T CD4+> ou égal à 200 cellules/µL) (voir la rubrique "Pharmacodynamie"). Le profil de tolérance a été globalement similaire à celui observé au cours du suivi du sous-groupe de surveillance des événements indésirables de l'étude SPS.
Les événements indésirables ont été suivis jusqu'à 42 jours après la vaccination et les événements indésirables graves pendant toute la période de l'étude (c'est à dire 180 jours). Parmi les 295 sujets ayant reçu ZOSTAVAX, un cas grave d'éruption maculopapuleuse lié au vaccin a été rapporté le 4ème jour suivant la 1ère dose de ZOSTAVAX (voir rubrique "Contre-indications").
Adultes séronégatifs VZV
Sur la base de données limitées provenant de deux études cliniques ayant inclus des sujets séronégatifs ou faiblement séropositifs vis-à-vis du VZV (âgés de 30 ans et plus) ayant reçu le vaccin zona vivant atténué, les effets indésirables au site d'injection et les effets systémiques ont été généralement similaires à ceux rapportés par d'autres sujets ayant reçu ZOSTAVAX au cours des essais cliniques, avec 2 sujets sur 27 ayant rapporté une fièvre. Aucun sujet n'a rapporté d'éruption de type varicelle ou zona. Aucun effet indésirable grave lié au vaccin n'a été rapporté.
1.5. Autres études
Adultes recevant une dose additionnelle / revaccination
Dans une étude clinique, des adultes de 60 ans et plus ont reçu une seconde dose de ZOSTAVAX 42 jours après la première dose (voir la rubrique "Pharmacodynamie"). La fréquence des effets indésirables liés au vaccin après la seconde dose de ZOSTAVAX a été globalement similaire à celle observée avec la première dose.
Dans une autre étude, ZOSTAVAX a été administré en dose de rappel à des sujets de 70 ans et plus sans antécédent de zona qui avaient reçu une première dose environ 10 ans auparavant et en première dose à des sujets de 70 ans ou plus sans antécédent de zona (voir rubrique "Pharmacodynamie"). La fréquence des effets indésirables liés au vaccin après la dose de rappel de ZOSTAVAX était généralement semblable à celle observée avec la première dose.
2. Effets sur l’aptitude à conduire des véhicules et à utiliser des machines
Les effets sur l’aptitude à conduire des véhicules et à utiliser des machines n’ont pas été étudiés. Cependant, il est attendu que ZOSTAVAX n'ait aucun effet ou un effet négligeable sur l'aptitude à conduire et utiliser des machines.
3. Surdosage
L'administration d'une dose plus élevée que la dose recommandée de ZOSTAVAX a été rarement rapportée et le profil des événements indésirables était comparable à celui observé avec la dose recommandée de ZOSTAVAX.
4. Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet :www.signalement-sante.gouv.fr.
Pharmacodynamie
Classe pharmacothérapeutique : Vaccins, Vaccin viral.
Code ATC : J07BK02.
1. Mécanisme d’action
Toute personne ayant été infectée par le VZVVZ, y compris celle n’ayant pas d’antécédent clinique connu de varicelle, est à risque de développer un zona. Ce risque semble lié à une baisse de l’immunité spécifique contre le VZV. ZOSTAVAX a montré qu’il relançait l’immunité spécifique anti-VZV, ce qui semble être le mécanisme par lequel il protège du zona et de ses complications (voir Immunogénicité).
2. Efficacité clinique
L'efficacité clinique de protection de ZOSTAVAX a été démontrée dans deux grandes études cliniques randomisées contrôlées contre placebo, pour lesquelles les sujets ont reçu ZOSTAVAX par voie sous-cutanée (voir les tableaux 1 et 2).
Etude d'efficacité et de tolérance de ZOSTAVAX (ZEST, ZOSTAVAX Efficacy and Safety Trial) chez les sujets de 50 à 59 ans
L'étude ZEST était un essai contrôlé en double aveugle contre placebo, dans lequel 22 439 sujets ont reçu une dose unique soit de ZOSTAVAX soit de placebo et ont été suivis pour la survenue d'un zona pendant une période médiane de 1,3 ans (intervalle de 0 à 2 ans). Le diagnostic de certitude des cas de zona a été réalisé par une Réaction de Polymérisation en Chaîne (PCR) [86 %] ou, en l'absence de détection de virus, par le comité d'évaluation clinique [14 %]. ZOSTAVAX a significativement réduit l'incidence du zona comparativement au placebo (voir Tableau 1).
Tableau 1 : efficacité de Zostavax sur l'incidence du zona comparativement au placebo dans l'étude ZEST chez les sujets de 50 à 59 ans *


Etude de Prévention du Zona (SPS : Shingles Prevention Study) chez les sujets de 60 ans et plus
L'étude SPS était un essai clinique en double aveugle contrôlé contre placebo qui a inclus 38 546 sujets, randomisés qui ont reçu soit une dose de ZOSTAVAX soit une dose de placebo et ont été suivis pour la survenue d'un zona pendant une période médiane de 3,1 ans (intervalle de 31 jours à 4,9 ans).
ZOSTAVAX a diminué de façon significative l'incidence du zona comparativement au placebo (voir tableau 2).
Tableau 2 : efficacité de Zostavax sur l'incidence du zona comparativement au placebo dans l'étude SPS chez les sujets de 60 ans et plus *


† Les groupes d'âge à la randomisation étaient de 60-69 ans et ≥ 70 ans.
Dans la SPS, la réduction des cas de zona a été constatée dans presque tous les dermatomes. Des cas de zona ophtalmique sont survenus chez 35 sujets vaccinés par ZOSTAVAX contre 69 chez les sujets ayant reçu un placebo. Une altération de la vision est survenue chez 2 vaccinés par ZOSTAVAX contre 9 chez les sujets ayant reçu un placebo.
ZOSTAVAX a diminué significativement l’incidence des névralgies post-zostériennes (NPZ) comparativement au placebo (voir tableau 3). Chez les sujets ayant présenté un zona, ZOSTAVAX a diminué le risque de développer des NPZ. Dans le groupe vacciné, le risque de développer des NPZ après un zona était de 9 % (27/135) contre 13 % dans le groupe placebo (80/642). Cette diminution était plus importante pour les sujets de plus de 70 ans, chez qui le risque de développer des NPZ suite à un zona a été réduit à 10 % dans le groupe vacciné contre 19 % dans le groupe placebo.
Tableau 3 : efficacité de ZOSTAVAX sur l'incidence des NPZ † comparativement au placebo dans l'étude SPS chez les sujets de 60 ans et plus *
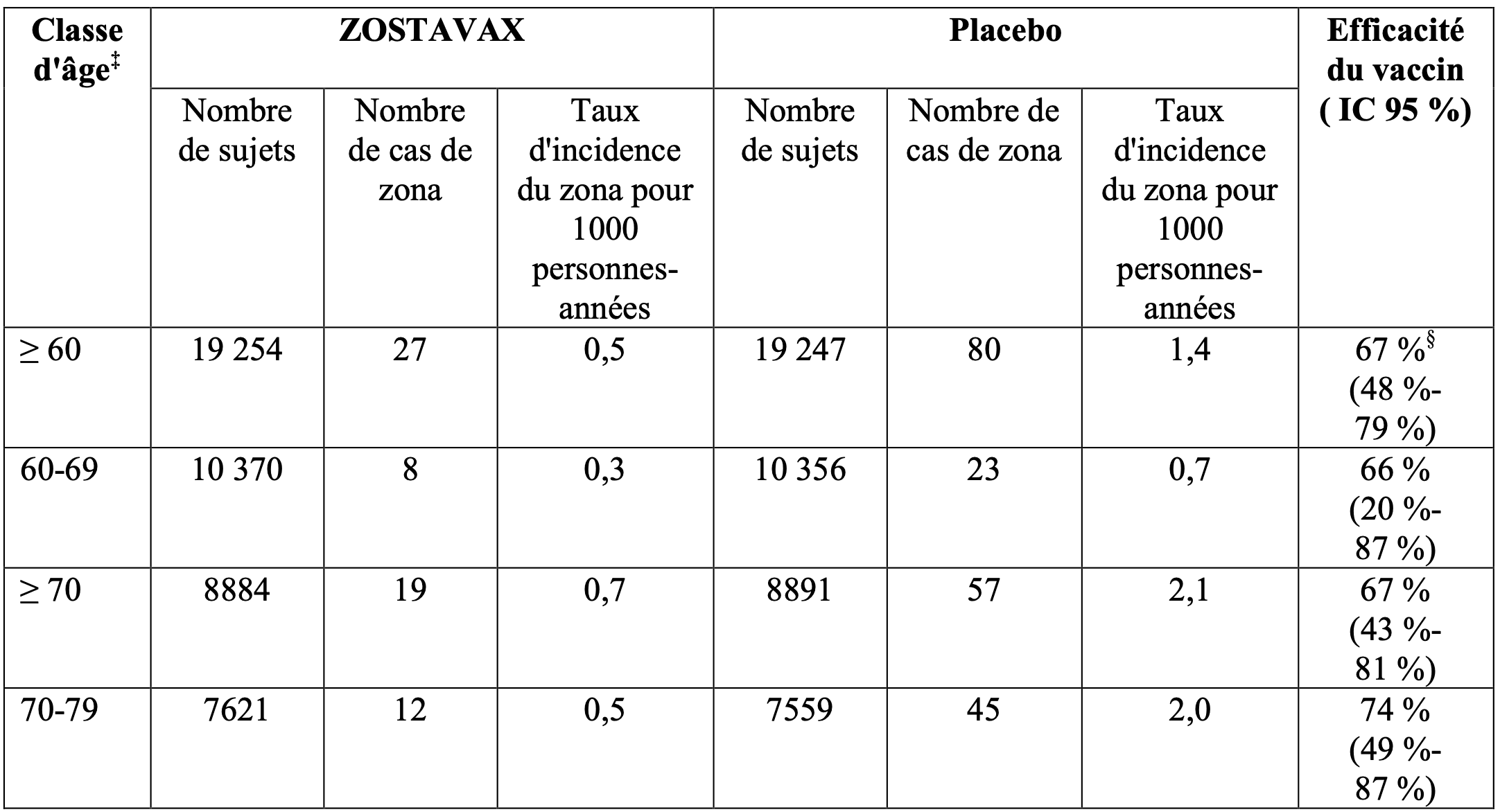

* Le tableau est basé sur la population en intention de traiter (ITT) qui comprenait tous les sujets randomisés dans l'étude, suivis au minimum 30 jours après la vaccination et n'ayant pas développé de cas de zona évaluable dans les 30 premiers jours après la vaccination ;
‡ Les groupes d'âge à la randomisation étaient de 60-69 ans et ≥ 70 ans ;
§ Estimation ajustée sur l'âge en fonction des classes d'âge (60-69 et ≥ 70 ans) à la randomisation.
ZOSTAVAX a réduit significativement le score de Sévérité des Douleurs associées au Zona (SDZ)(voir tableau 4).
Tableau 4 : réduction des douleurs associées au zona par le SDZ chez les sujets de 60 ans et plus *


‡ Les groupes d'âge à la randomisation étaient de 60-69 ans et ≥ 70 ans.
3. Prévention des cas de zona avec douleurs intenses dans la population totale de l’étude SPS
ZOSTAVAX a réduit l’incidence du zona avec douleurs intenses et de longue durée (score de sévérité-durée >600) de 73 % (IC à 95 % : 46 à 87 %) par rapport au placebo (respectivement, 11 cas contre 40).
4. Diminution du score de sévérité-durée des douleurs associées au zona chez les sujets vaccinés qui ont présenté un zona
Il n’y a pas de différence statistiquement significative entre le groupe vacciné et le groupe placebo, pour les douleurs aiguës (douleur d’une durée de 0 à 30 jours).
Cependant, chez les sujets vaccinés ayant développé des NPZ, ZOSTAVAX a réduit de façon significative les douleurs chroniques associées aux NPZ par rapport au placebo. Sur la période allant du 90ème jour après l’éruption jusqu’à la fin du suivi, une diminution de 57% du score de sévérité-durée a été observée (score moyen de 347 pour ZOSTAVAX et de 805 pour le placebo, p=0,016).
Globalement, chez les sujets vaccinés ayant développé un zona, ZOSTAVAX a diminué de façon significative les douleurs aiguës et chroniques associées au zona par rapport au placebo. Sur une période de suivi de 6 mois des douleurs aiguës et chroniques, une diminution de 22 % (p=0,008) du score de sévérité-durée a été observée, ainsi qu’une diminution de 52 % (IC à 95 % : 7 à 74 %) du risque de développer un zona avec des douleurs intenses et de longue durée de 6,2 % à 3,5 %, (score de sévérité-durée >600).
5. Persistance de la protection par ZOSTAVAX
La persistance de la protection après la vaccination a été évaluée au moyen de la sous-étude de la persistance à court terme (STPS: Short-Term Persistence Substudy) et de la sous-étude de persistance à long terme (LTPS : Long-Term Persistence Substudy ) et soutient le bénéfice continu de ZOSTAVAX au cours des périodes de suivi étudiés. La STPS a été initiée pour obtenir des informations complémentaires sur la persistance de l'efficacité du vaccin chez les sujets ayant reçu ZOSTAVAX lors de la SPS.
La persistance de l'efficacité de ZOSTAVAX a été étudiée 4 à 7 ans après la vaccination dans le cadre de la STPS, qui a inclus 7 320 sujets préalablement vaccinés par ZOSTAVAX et 6 950 sujets ayant préalablement reçu un placebo au cours de la SPS (l'âge moyen lors de l'inclusion était de 73,3 ans) ; et 7 à 10 ans après la vaccination dans le cadre de la sous-étude de persistance à long terme (LTPS), qui a inclus 6 867 sujets préalablement vaccinés par ZOSTAVAX (l'âge moyen lors de l'inclusion était de 74,5 ans). La médiane de suivi était d'environ 1,2 an (intervalle 1 jour à 2,2 ans) etenviron 3,9 ans (intervalle d'1 semaine à 4,75 ans) respectivement dans la STPS et LTPS.
Au cours de la STPS, ZOSTAVAX a été proposé aux sujets ayant reçu le placebo, date à laquelle ils ont été considérés comme ayant terminé la STPS. Un contrôle placebo concomitant n'était plus disponible dans la LTPS ; des données provenant du groupe placebo initial ont été utilisées pour estimer l'efficacité du vaccin.
Dans la STPS, il y a eu 84 cas de zona évaluables [8,4 / 1000 personnes-années] dans le groupe ZOSTAVAX et 95 cas évaluables [14,0 / 1000 personnes-années] dans le groupe placebo. L'efficacité vaccinale estimée au cours de la période de suivi de la STPS a été de 40 % (IC95 % : [18 % à 56 %]) pour l'incidence du zona, de 60 % (IC95 % : [-10 % à 87 %]) pour l'incidence des NPZ et de 50 % (IC95 % : [14 % à 71 %]) pour le score de sévérité du zona (score SDZ).
Dans la LTPS, il y avait 263 cas évaluables de zona signalés parmi 261 patients [10,3 / 1000 personnes-années]. L'efficacité vaccinale estimée au cours de la période de suivi de la LTPS a été de 21 % (IC 95 % : [11 à 30 %]) pour l'incidence du zona, de 35 % (IC 95 % : [9 à 56 %]) pour l'incidence des NPZ et de 37 % (IC 95 % : [27 à 46 %]) pour le score SDZ.
Etude d’efficacité en vie réelle à long terme, chez des personnes de 50 ans et plus
Dans une étude de cohorte observationnelle prospective, de grande échelle, d’efficacité à long terme de ZOSTAVAX en vie réelle, aux Etats Unis, des personnes âgées de 50 ans ou plus au moment de la vaccination étaient suivies pour la survenue de zona et de NPZ à l'aide de critères d'évaluation validés.
Sur les 1 505 647 sujets de l’étude, 507 444 ont reçu ZOSTAVAX entre 2007 et 2018. Un total de75 135 cas confirmés de zona et 4 954 cas confirmés de NPZ (douleur associée au zona > 90 jours) ont été observés. Les résultats ont montré que ZOSTAVAX est efficace pour réduire l’incidence du zona et des NPZ pendant plus de 8 à 10 ans chez les personnes vaccinées comparativement au groupe de référence de non vaccinés.
L’efficacité du vaccin (EV) contre le zona estimée par âge au moment de la vaccination et l’EV moyenne estimée sur les 3, 5, 8 et 10 premières années post-vaccination sont présentées dans le tableau ci-dessous (voir Tableau 5).
Tableau 5 : EV † de ZOSTAVAX contre le zona sur la période de l’étude de 2007 à 2018 et en moyenne sur 3, 5, 8 et 10 ans, par âge au moment de la vaccination


* Modèles Cox ajustés pour le temps calendaire, l’âge, le sexe, le groupe racial/ethnique, l’utilisation de ressource de santé (vaccination contre la grippe, nombre de semaines avec consultation externe par an), comorbidités (score DxCG, score de risque HCUP), statut du déficit immunitaire pendant la période de suivi ;
‡ L’EV sur la période de l’étude est l’EV calculée sur toute la durée de l’étude (2007-2014) au moment de l’analyse intermédiaire ;
§ : l’EV moyenne a été calculée comme la moyenne pondérée des estimations des EV annuelles sur respectivement 3 et 5 ans, où les poids sont proportionnels à la période totale couverte ;
¶ Données non disponibles ;
Abréviations : EV efficacité du vaccin, IC intervalle de confiance, DxCG groupe coût et diagnostic, HCUP projet de coût et utilisation des ressources de santé.
L’EV contre les NPZ estimée par âge au moment de la vaccination et l’EV moyenne estimée sur les 3, 5 et 8 premières années après la vaccination sont présentées ci-dessous (voir Tableau 6).
Tableau 6 : EV † de ZOSTAVAX contre les névralgies post-zostériennes (NPZ) sur la période de l’étude de 2007 à 2018 et en moyenne sur 3, 5 et 8 ans, par âge au moment de la vaccination


* Modèles Cox ajustés pour le temps calendaire, l’âge, le sexe, le groupe racial/ethnique, l’utilisation de ressource de santé. (vaccination contre la grippe, nombre de semaines avec consultation externe par an), comorbidités (score DxCG, score de risque HCUP), statut du déficit immunitaire pendant la période de suivi ;
‡ L’EV sur la période de l’étude est l’EV calculée sur toute la durée de l’étude (2007-2014) au moment de l’analyse intermédiaire ;
§ L’EV moyenne a été calculée comme la moyenne pondérée des estimations des EV annuelles sur 3 et 5 ans, respectivement, ou les poids sont proportionnels à la période totale couverte ;
¶ Données non disponibles ;
Abréviations : EV efficacité du vaccin, IC intervalle de confiance, DxCG groupe diagnostic et coût, HCUP projet de coût et utilisation des ressources de santé.
6. Immunogénicité de ZOSTAVAX
Etude de Prévention du Zona (SPS, Shingles Prevention Study)
Dans l'étude SPS, les réponses immunitaires à la vaccination ont été évaluées dans un sous-groupe (N=1395). Six semaines après la vaccination, ZOSTAVAX a induit des réponses immunitaires spécifiques au VZV significativement plus élevées que celles induites par le placebo.
Etude d'efficacité et de tolérance de ZOSTAVAX (ZEST, ZOSTAVAX Efficacy and Safety Trial)
Dans l'étude ZEST, les réponses immunitaires à la vaccination ont été évaluées dans un sous groupe randomisé correspondant à 10% (n=1 136 pour ZOSTAVAX et n=1 133 pour le placebo) des sujets inclus dans ZEST. Six semaines après la vaccination, ZOSTAVAX a induit des réponses immunitaires spécifiques au VZV significativement plus élevées comparativement au placebo.
Lors de l'évaluation réalisée 4 semaines après la vaccination, l'immunogénicité de la formulation réfrigérée actuelle, est apparue similaire à l'immunogénicité de la précédente formulation congelée de ZOSTAVAX.
Les sujets ayant reçu ZOSTAVAX par voie SC (sous-cutanée) ou IM (intramusculaire)
Dans une étude ouverte, randomisée, contrôlée, ZOSTAVAX a été administré soit par voie SC soit par voie IM à 353 sujets de 50 ans et plus. Les sujets présentant une thrombocytopénie sévère ou tout autre trouble de la coagulation étaient exclus. La réponse immunitaire VZV spécifique à ZOSTAVAX était comparable 4 semaines après la vaccination, que la voie d'administration ait été en SC ou IM.
Administration concomitante
Dans une étude clinique contrôlée en double aveugle, 762 adultes de 50 ans et plus ont été randomisés pour recevoir une dose de ZOSTAVAX administrée de façon concomitante (n= 382) ou non concomitante (n= 380) avec un vaccin grippal inactivé à virion fragmenté. Quatre semaines après vaccination, la réponse immunitaire VZV spécifique était similaire, que les vaccins soient administrés ou non de façon concomitante.
Dans une étude clinique contrôlée en double aveugle, 473 adultes de 60 ans et plus ont été randomisés pour recevoir une dose de ZOSTAVAX administrée de façon concomitante (n=237) ou non concomitante (n=236) avec un vaccin pneumococcique polyosidique comportant 23 valences. Quatre semaines après vaccination, la réponse immunitaire VZV spécifique suite à une administration concomitante n'était pas similaire à la réponse immunitaire VZV spécifique observée suite à une administration non concomitante. Toutefois, dans une étude de cohorte d'efficacité en vie réelle menée aux Etats-Unis chez 35 025 adultes de 60 ans et plus, aucune augmentation du risque de zona n'a été observée chez les sujets vaccinés en même temps par ZOSTAVAX et le vaccin pneumococcique polyosidique 23-valent (n=16 532) comparativement aux sujets vaccinés par ZOSTAVAX un mois à un an après le vaccin pneumococcique polyosidique 23-valent (n=18 493) en pratique courante. Le rapport des risques (Hazard Ratio) ajusté comparant le taux d'incidence du zona dans les deux groupes était de 1,04 (IC à 95%, 0,92, 1,16) sur un suivi médian de 4,7 ans. Les données n'indiquent pas que l'administration concomitante des deux vaccins altère l'efficacité en vie réelle de ZOSTAVAX.
Sujets ayant un antécédent de zona avant la vaccination
Dans un essai clinique en double aveugle, randomisé, controlé contre placebo, ZOSTAVAX a été administré à 100 sujets de 50 ans et plus avec un antécédent de zona afin d'évaluer l'immunogénicité et la tolérance (voir rubrique "Effets indésirable") de ZOSTAVAX. ZOSTAVAX a induit une réponse immunitaire spécifique au VZV, 4 semaines après la vaccination, comparativement au placebo. La réponse immunitaire VZV spécifique était généralement similaire entre les sujets de 50 à 59 ans et ceux de 60 ans et plus.
Sujets ayant reçu une dose additionnelle / revaccination
La nécessité, ou le délai, d'une dose de rappel par ZOSTAVAX n'ont pas encore été déterminés. Dans une étude ouverte, ZOSTAVAX a été administré comme : (1) dose de rappel à 201 sujets de 70 ans ou plus sans antécédent de zona qui avaient reçu une première dose environ 10 ans auparavant en tant que participants à l'étude de Prévention du Zona (SPS), et (2 ) première dose à 199 sujets de 70 ans ou plus sans antécédent de zona. La réponse immunitaire VZV spécifique au vaccin 6 semaines après la vaccination était comparable entre le groupe recevant la dose de rappel et le groupe recevant la première dose.
Sujets sous traitement d'entretien ou chronique par corticoïdes
Dans une étude clinique randomisée en double aveugle contrôlée contre placebo, ZOSTAVAX a été administré à 206 sujets de 60 ans ou plus recevant un traitement d'entretien ou chronique par corticoïdes à une dose quotidienne équivalente à 5 à 20 mg de prednisone, initié au moins 2 semaines avant l'inclusion et poursuivi au moins 6 semaines après la vaccination afin d'évaluer l'immunogénicité et la tolérance de ZOSTAVAX. Comparativement au placebo, ZOSTAVAX induit une réponse immunitaire VZV spécifique plus élevée 6 semaines après la vaccination.
Adultes infectés par le VIH avec une fonction immunitaire conservée
Dans une étude clinique randomisée en double aveugle contrôlée contre placebo, ZOSTAVAX a été administré à des adultes infectés par le VIH (18 ans ou plus; âge médian 49 ans) sous traitement anti-rétroviral approprié avec une fonction immunitaire conservée (nombre de lymphocytes T CD4 + ≥200 cellules / µL). Bien que, ZOSTAVAX soit indiqué en une seule dose (voir rubrique "Posologie"), un schéma à deux doses a été utilisé. 286 sujets ont reçu deux doses et 9 sujets ont reçu une seule dose.Les réponses immunitaires VZV spécifiques après administration de doses 1 et 2 étaient similaires (voir rubrique "Contre-indications").
7. Sujets immunodéficients
Le vaccin n’a pas été évalué chez les sujets présentant un déficit immunitaire.
L'Agence européenne des médicaments a renoncé à l'obligation de soumettre les résultats d'études réalisées avec ZOSTAVAX dans tous les sous-ensembles de la population pédiatrique (voir rubrique "Posologie" pour les informations concernant l'usage pédiatrique).
Conservation
Durée de conservation : 18 mois.
A conserver et transporter réfrigéré (entre 2 °C et 8 °C).
Ne pas congeler.
Après reconstitution, le vaccin doit être utilisé immédiatement. Cependant, la stabilité a été démontrée pendant 30 minutes si conservé à 20 °C - 25 °C.
Conserver dans l’emballage d'origine à l'abri de la lumière.
Manipulation
Avant d’être mélangée avec le solvant, la poudre du vaccin est un agglomérat compact et cristallin, blanc à blanc cassé. Le solvant est un liquide clair et incolore. Une fois reconstitué, ZOSTAVAX est un liquide légèrement trouble à translucide, de blanc cassé à jaune pâle.
Eviter les contacts avec les désinfectants car ils peuvent inactiver le virus vaccinal.
Pour reconstituer le vaccin, utiliser le solvant fourni. Après reconstitution, ZOSTAVAX est un liquide légèrement trouble à translucide, de blanc cassé à jaune pâle.
Il est important d'utiliser une seringue et une aiguille stériles, distinctes pour chaque patient afin de prévenir la transmission d'agents infectieux d'un patient à un autre.
Une aiguille doit être utilisée pour la reconstitution et une autre nouvelle aiguille pour l’injection.
L'administration du vaccin doit être consignée par le médecin sur le carnet de vaccination ou de santé avec le numéro de lot. Il peut aussi être inscrit par le patient ou son médecin sur un carnet de vaccination numérique (version grand public ou professionnelle).
En l’absence d’études de compatibilité, ce vaccin ne doit pas être mélangé avec d’autres médicaments.
Instructions pour la reconstitution
ZOSTAVAX avec un solvant pour reconstitution fourni en flacon
- Prélever la totalité du contenu du flacon de solvant dans une seringue.
- Injecter la totalité du contenu de la seringue dans le flacon contenant la poudre.
- Agiter doucement afin de dissoudre complètement.
Le vaccin reconstitué doit être inspecté visuellement pour mettre en évidence la présence de particules et / ou une apparence physique anormale avant administration. Dans l’un ou l’autre de ces cas, le vaccin doit être jeté.
Il est recommandé d’administrer le vaccin immédiatement après reconstitution afin de minimiser la perte d’activité. Jeter le vaccin reconstitué s’il n’est pas utilisé dans les 30 minutes.
Ne pas congeler le vaccin reconstitué.
Prélever la totalité du contenu du vaccin reconstitué dans le flacon avec une seringue, changer l’aiguille et injecter la totalité du volume par voie sous-cutanée ou intramusculaire.
ZOSTAVAX avec un solvant pour reconstitution fourni en seringue préremplie
- Pour fixer l’aiguille, elle doit être fermement montée sur l’embout de la seringue et sécurisée en la tournant d’un quart de tour (90 °).
- Injecter la totalité du contenu de la seringue de solvant dans le flacon contenant la poudre. Agiter doucement afin de dissoudre complètement.
Le vaccin reconstitué doit être inspecté visuellement pour mettre en évidence la présence de particules et / ou une apparence physique anormale avant administration. Dans l’un ou l’autre de ces cas, le vaccin doit être jeté.
Il est recommandé d'administrer le vaccin immédiatement après reconstitution, afin de minimiser la perte d'activité. Jeter le vaccin reconstitué s'il n'est pas utilisé dans les 30 minutes.
Ne pas congeler le vaccin reconstitué.
Prélever la totalité du contenu du vaccin reconstitué dans le flacon avec une seringue, changer l’aiguille et injecter la totalité du volume par voie sous-cutanée ou intramusculaire.
L'administration du vaccin doit être consignée par le médecin sur le carnet de vaccination ou de santé avec le numéro de lot. Il peut aussi être inscrit par le patient ou son médecin sur un carnet de vaccination électronique.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Autres informations
Données de sécurité préclinique
Les études non cliniques conventionnelles de sécurité n'ont pas été effectuées, mais il n’y a pas d’inquiétude au plan préclinique qui puisse être pertinente vis à vis de la sécurité clinique au-delà des données déjà fournies dans d’autres rubriques du Résumé des Caractéristiques du Produit (RCP).
Remboursement
Remboursé par la Sécurité sociale à 30% dans la seule indication :
- prévention du zona et des douleurs postzostériennes des personnes âgées de 65 à 74ans révolus selon un schéma à une dose.
Cette présentation est agréée aux collectivités.